论文亮点
陈钊 hLife Journal2024-05-08 07:15北京
本文系统地总结了G蛋白偶联受体(G-protein coupled receptors, GPCRs)别构位点的结构信息和调控功能机制,并且梳理了目前已经发表的基于GPCRs结构的虚拟筛选(Structure-based virtual screening, SBVS)研究,深入探讨了靶向GPCRs别构位点进行药物虚拟筛选和设计所具有的广阔前景以及面临的挑战。
论文导读
北京生命科学研究所/清华大学生物医学交叉研究院黄牛研究团队在hLife上发表了题为“Exploring structure-based drug discovery of GPCRs beyond the orthosteric binding site”的综述。文章总结了目前已知结构GPCR的别构位点及其调节机制,在总结靶向正构位点药物虚拟筛选成功经验的基础上,重点探讨了别构位点调控剂的发展潜力,并且特别强调了容易被忽视的细胞膜组分在针对别构位点进行虚拟筛选过程中的重要性,同时文章也通过实例说明了超大规模或专用化合物库在发现新型小分子配体以及AI在加速虚拟筛选速度中的重要价值。

扫码阅读原文
GPCRs是药物发现中最重要和最成功的靶点,近年来针对GPCRs正构位点进行的虚拟筛选已经广泛开展。随着GPCRs别构位点结构和功能研究的深入开展,靶向GPCRs别构位点进行的新药研发也越来越受到关注。然而,靶向GPCRs别构位点的虚拟筛选面临诸多挑战,除了进一步拓展和完善别构位点的结构信息之外,如何分析和描述别构位点、小分子配体,以及膜组分三者之间的相互作用,对朝向细胞膜环境别构位点的虚拟筛选至关重要。同时,如何快速准确地筛选到全新结构类型的配体也是亟待解决的重要技术问题。
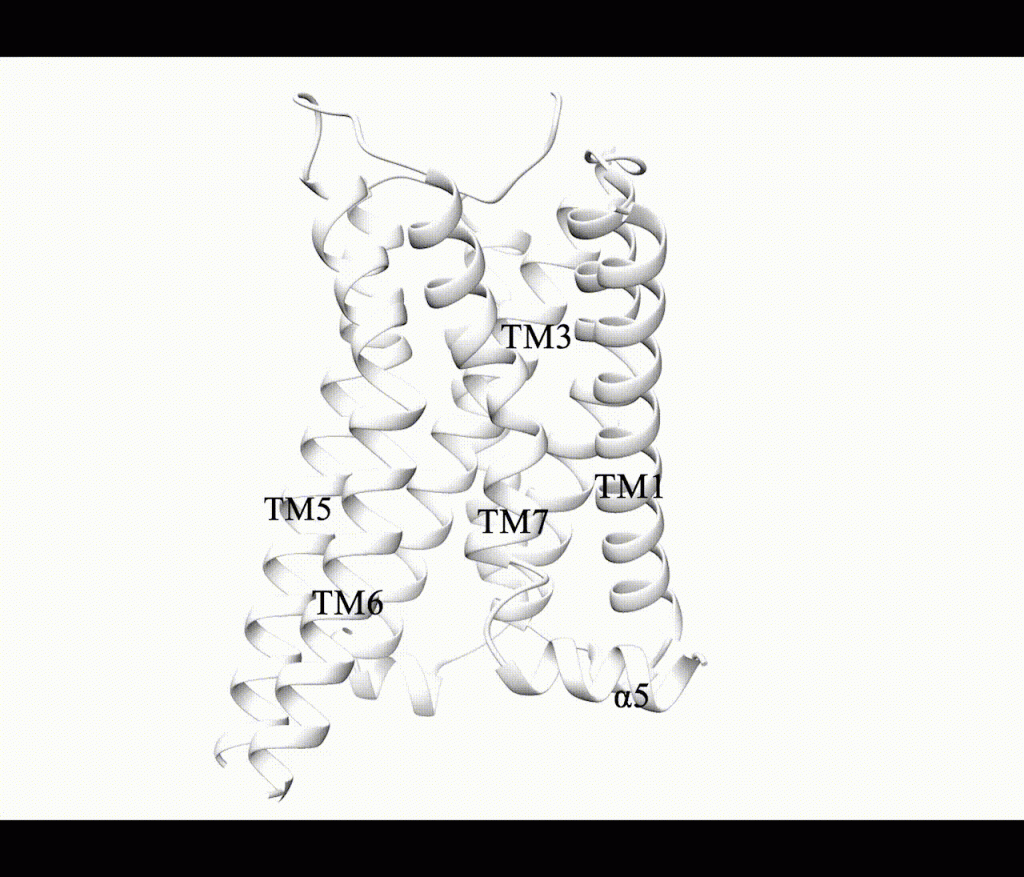
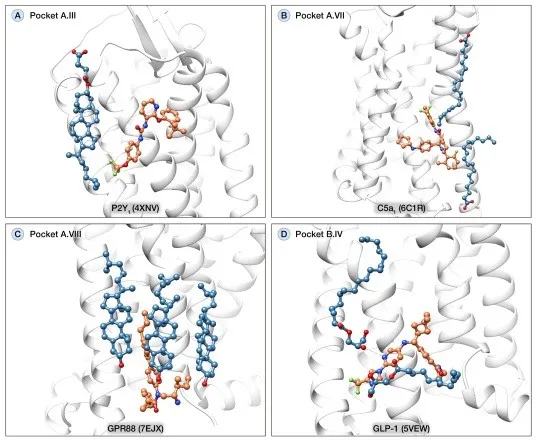
文章首先收集整理了A、B、C、F四类GPCRs中已知结构的变构位点信息,根据位点的位置以及具体的变构机制进行了划分(图1-3)。这些别构位点主要分布在四个区域:(1)正构位点上方,结合在该位置的别构调节剂主要影响激动剂或者拮抗剂的结合或解离速率;(2)七次跨膜螺旋外部与细胞膜的交界处,大部分别构位点都在这一区域,结合在这些位点上的变构调节剂通过疏水相互作用稳定跨膜螺旋的交界面,从而影响GPCRs的构象转变;(3)七次跨膜螺旋内部(在C类GPCRs中最常见)以及(4)GPCRs的胞内区域,结合在这两个区域的小分子不仅影响跨膜螺旋的重排,同时也稳定了GPCRs与α5螺旋的相互作用,从而影响G蛋白偶联。
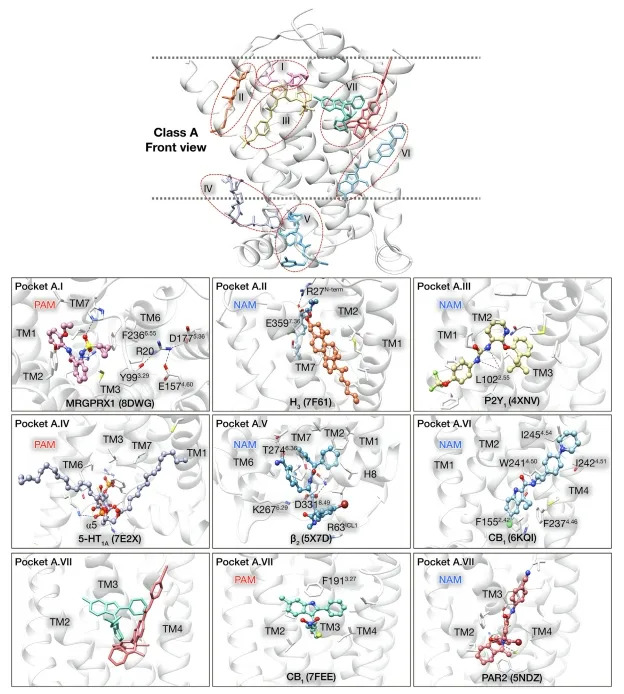
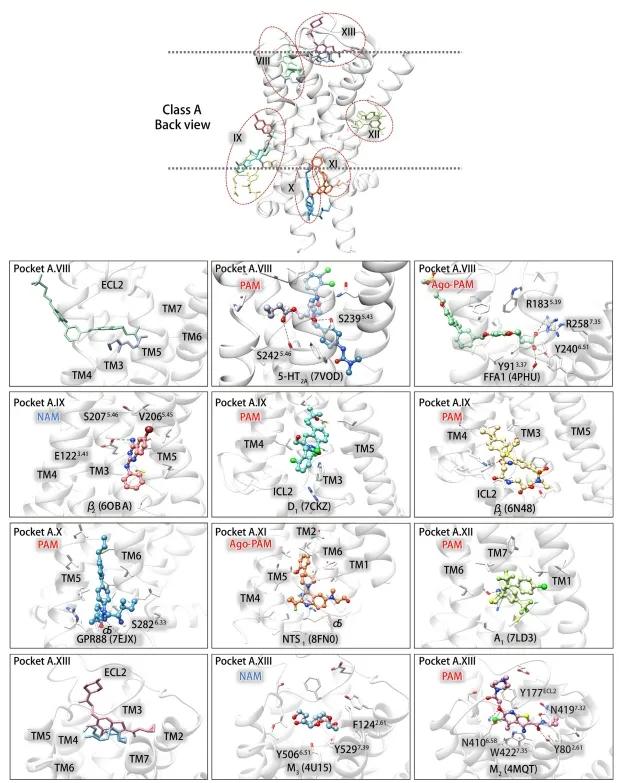
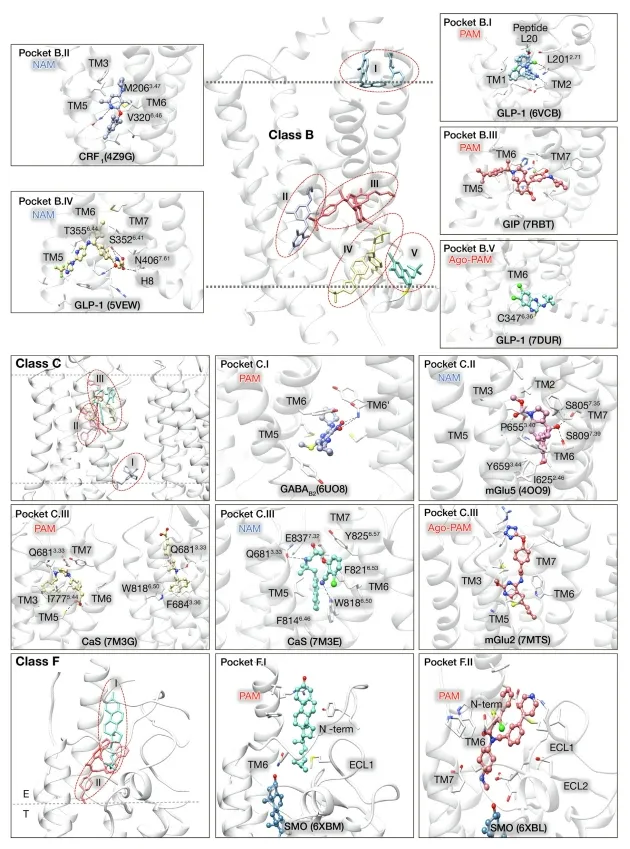
随着GPCRs别构位点结构数据的增长,靶向GPCRs变构位点药物的筛选和发现也逐渐得到了大家的关注。文章统计了目前已经发表且有可信实验数据的基于GPCRs结构的虚拟筛选研究(总计72篇)。由于正构位点较为丰富的结构信息和清楚的调节机制,基于正构位点结构进行虚拟筛选目前是研究的主流(68篇)。靶向变构位点的虚拟筛选的研究数量则相对较少(4篇),并且对位点的选择都集中在正构位点上方和跨膜螺旋内,其他区域的别构位点结构,尤其是大量位于七次跨膜螺旋外部与细胞膜交界处的别构位点,并没有被很好地利用起来,存在巨大潜力。
同时,文章也讨论了超大规模分子库以及专用分子库在全新的药物分子类型发现中的重要作用。如LYU等使用1.38亿大小的分子库对D1受体进行了虚拟筛选,筛选出81个新的分子类型,其中30个具有亚微摩尔级别的活性。另一方面,Shoichet等构建了一个定制的含有四氢吡啶骨架的分子库,在靶向5-HT2A的虚拟筛选中也取得了很好的表现。
近几年来,随着AI技术的快速发展,AI方法在加速GPCRs药物发现方面的应用也在显著增长。一方面,生成式模型被应用于构建分子库,而AlphaFold2使得准确预测GPCRs结构成为可能,两者拓展了SBVS的化学空间和靶点数量,另一方面,AI也可以帮助快速地对超大规模分子库进行初步筛选,从而加快筛选速度。
最后,文章展望了位于跨膜螺旋和细胞膜交界处的别构位点在GPCRs药物发现中的研究潜力和需要解决的问题。目前已知的GPCRs别构位点大部分都邻接细胞膜(图4),针对这些位点进行药物筛选和开发有着巨大的研究潜力和价值。然而在大部分GPCRs结构中这些细胞膜组分的信息是缺失的,因此如何通过合理的计算手段去模拟评估脂质分子对小分子结合的影响是靶向这些别构位点进行虚拟筛选的亟需解决的难题。
总体而言,从新药研发历史来看,约有35%的FDA批准上市药物是靶向GPCRs,但其中(绝)大部分都是通过传统的药物筛选和研发模式找到。如何在低悬果实已被传统药物筛选摘取后做出新意?近年来GPCRs蛋白结构解析日新月异,极大拓展了对GPCR激活和拮抗机理机制的认知,譬如偏向性信号传导与GPCR蛋白不同构象状态紧密相关。古人常说,“非常之观,常在于险远。有志矣,不随以止也,然力不足者,亦不能至也。”这里的力,在GPCRs或许就是别构之力。深入解读GPCR蛋白三维结构提供的新维度信息,尤其是别构位点信息,利用小分子化合物和别构位点的作用力,诱导GPCR蛋白新构象,探索GPCR蛋白新机制,踏上奇伟、瑰怪的惊喜之旅。
✦
作者简介

机构:北京生命科学研究所/清华大学生物医学交叉研究院
研究方向:计算机辅助药物设计

机构:北京生命科学研究所/北京师范大学生命科学学院
研究方向:计算机辅助药物设计

机构:北京生命科学研究所

研究方向:计算机辅助药物设计
机构:北京生命科学研究所/清华大学生物医学交叉研究院
研究方向:计算机辅助药物设计
引用格式:Chen Z, Ren X, Zhou Y, et. al. Exploring structure-based drug discovery of GPCRs beyond the orthosteric binding site. hLife.
